
Borstkanker
|
|
Neem het voorbehoud bij medische informatie in acht. Raadpleeg bij gezondheidsklachten een arts. |
| Borstkanker | ||||
|---|---|---|---|---|
| Mammacarcinoom | ||||

| ||||
| Synoniemen | ||||
| Latijn | Carcinoma mammae | |||
| Nederlands | Borstkliercarcinoom | |||
| Coderingen | ||||
| ICD-10 | C50 | |||
| ICD-9 | 174-175 | |||
| OMIM | 114480 | |||
| DiseasesDB | 1598 | |||
| MedlinePlus | 000913 | |||
| eMedicine | med/2808 | |||
| ||||
Borstkanker of mammacarcinoom is een vorm van kanker die uitgaat van het melkklierweefsel in de borst. Het is de meest voorkomende soort kanker bij vrouwen: 22 procent van alle kankers bij vrouwen. Jaarlijks treft het wereldwijd ongeveer 1 miljoen vrouwen. In België en Nederland krijgt één op de negen vrouwen borstkanker. Ter vergelijking: in de VS is dat 1 op de 8. Onder vrouwen tussen 30 en 59 jaar is het de meest voorkomende doodsoorzaak. Ten onrechte wordt soms verondersteld dat vrouwen bij wie geen borstkanker in de familie voorkomt een laag risico lopen. Het grootste deel (circa 75%) van de nieuwe gevallen van borstkanker wordt vastgesteld bij vrouwen bij wie de ziekte niet in de familie voorkomt.
Daar mannen ook een kleine hoeveelheid borstklierweefsel bezitten, kunnen ook zij borstkanker krijgen, al komt dat wel veel minder vaak voor. De kans dat een man borstkanker ontwikkelt is ongeveer 1 op 100.000 per jaar. In het hele leven is dat ongeveer 1:1000, honderdmaal minder vaak dan vrouwen.
Inhoud
Ontstaan
Borstkanker wordt veroorzaakt door afwijkingen in het DNA, mutaties die ervoor zorgen dat een cel (in dit geval een cel in de borst) ongecontroleerd gaat delen en groeien. Typerend voor kanker is dat de kankercellen hierbij ook het omringende, normale weefsel wegduwen, verdrukken en hinderen, en dat de cellen uiteindelijk kunnen uitzaaien naar andere plaatsen in het lichaam, waar ze uitzaaiingen (metastasen) gaan vormen.
De ontwikkeling van gewone cel naar kankercel is een proces met verschillende stadia. Risicofactoren beïnvloeden de kans dat een gewone borstcel zich uiteindelijk zal ontwikkelen tot kankercel.
Risicofactoren
Leeftijd
De kans op borstkanker wordt voor een belangrijk deel bepaald door de leeftijd, vrouwen op hogere leeftijd hebben een grotere kans op borstkanker.
Hormonale invloeden
Bij borstkanker is ook een belangrijke rol weggelegd voor hormonale invloeden. Een vrouw loopt meer risico op borstkanker:
- bij vroege menarche (eerste menstruatie 12 jaar of jonger);
- bij late menopauze (55 jaar of ouder);
- als zij op late leeftijd voor het eerst zwanger werd (ouder dan 35 jaar) of nooit zwanger was;
- bij geen of zeer kortdurend borstvoeding geven. Langdurig borstvoeding geven (tussen 4 en 12 maanden) kan de kans op borstkanker bij westerse vrouwen met 22% verlagen;
- bij gebruik van de anticonceptiepil ('de pil'): 24% verhoogd risico, 1-4 jaar gestopt: 16% verhoogd risico, 5-9 jaar gestopt: 7% hoger risico;
- als zij langer dan vier jaar hormoonvervangingstherapie gebruikt voor klachten tijdens de menopauze; dit verhoogt het risico met 20-40%, bij een preparaat met oestrogeen en een progestageen is dit veel hoger: 90-210%;
- bij overgewicht na de menopauze (vetweefsel produceert namelijk vrouwelijke hormonen) geschatte verhoging van het risico 30-50%.
Erfelijke invloed
Door middel van tweelingonderzoek is vastgesteld dat ongeveer 27% van de gevoeligheid voor het ontwikkelen van borstkanker veroorzaakt wordt door genetische risicofactoren. Desondanks komt de ziekte slechts bij ongeveer 15% van alle borstkankerpatiënten in de familie voor. Als borstkanker in de familie voorkomt, is de kans op het krijgen van borstkanker verhoogd. Wanneer één eerstegraads verwant is gediagnosticeerd met borstkanker (meestal dus de moeder, een zus of een dochter), heeft een vrouw ongeveer tweemaal zoveel kans dat zij ook borstkanker zal krijgen (dus circa 20% kans in plaats van de normale 10% kans).
Wanneer in een familie meerdere vrouwen op jongere leeftijd borstkanker hebben gekregen, kan men DNA laten onderzoeken op mutaties in de bekende borstkankergenen. Hiervoor verwijst de huisarts of oncoloog familieleden door naar de polikliniek van de afdeling Klinische Genetica (in België een Centrum voor Menselijke Erfelijkheid) van een ziekenhuis. Op basis van de aanwezigheid van familieleden met borstkanker en/of een gevonden mutatie kan besloten worden om de borsten regelmatig te controleren met behulp van MRI-scans of mammografie. Daarnaast is het preventief verwijderen van borsten en/of eierstokken een optie.
BRCA1 (op chromosoom 17) en BRCA2 (op chromosoom 13) zijn de twee belangrijkste borstkankergenen. Een vrouw met een mutatie (afwijking) in BRCA1 heeft een kans van 87 procent om borstkanker te krijgen voor haar 70e. Naast BRCA1 en BRCA2 zijn ook mutaties in P53 (Li-Fraumeni syndroom), PTEN (Cowden syndroom) en STK11 (Syndroom van Peutz-Jeghers) gelinkt aan een verhoogd risico op borstkanker. Mutaties in deze genen zijn echter zeer zeldzaam en worden bijna nooit gevonden in families die niet ook andere kenmerken van de betreffende syndromen hebben. Ten slotte geven ook mutaties in de genen ATM, CHEK2, BRIP1, PALB2 en NBS1 een verhoogde kans op borstkanker. Overigens zijn nog niet alle oorzaken van erfelijke borstkanker gevonden.
Geografische verschillen
Een westerse vrouw heeft vier keer meer kans op borstkanker dan een vrouw uit Afrika of Azië.
Overige risicofactoren
- Vlees in zijn algemeenheid, maar vooral rood vlees (bijvoorbeeld alle rund-, kalfs-, varkens- en lamsvleessoorten) en verwerkt vlees (ham, salami, bacon, leverpaté etc.) verhoogt het risico op borstkanker. Een belangrijke kankerpromotor in rood vlees is waarschijnlijk het heem-ijzer.
- Alcohol. Naarmate er meer alcohol wordt geconsumeerd, stijgt het risico op borstkanker. Alcohol heeft een verhogend effect op de androgeen en oestrogeenniveaus in het bloed.
- roken
- bepaalde soorten straling op het borstweefsel vergroten ook de kans op borstkanker. Ook de straling waaraan wordt blootgesteld bij mammografie bij het screenen op borstkanker kan het risico op borstkanker verhogen. Om deze reden moet voorzichtig met deze vorm van diagnostiek worden omgegaan.
- Het ondergaan hebben van een abortus of een miskraam blijkt geen invloed te hebben op de kans op borstkanker.
- Onvoldoende lichamelijke activiteit. Lichaamsbeweging kan het borstkankerrisico verminderen door een oestrogeenverlagend effect. De schattingen van de risicoreductie door lichaamsbeweging lopen uiteen van 20 tot 80 procent. Hoewel het effect is gevonden voor vrouwen van iedere leeftijd, lijkt er een extra beschermende invloed te zijn van lichaamsbeweging gedurende de adolescentie en jonge volwassenheid (12-24 jaar).
- Onvoldoende inname omega 3-vetzuren: Onder vrouwen die gedurende een periode van 10 jaar visoliecapsules gebruikten, blijkt het risico op een ductaal carcinoom, de meest voorkomende vorm van borstkanker met 32% verminderd te zijn. Een hoge consumptie van transvetzuren gaat juist gepaard met een hoger risico op borstkanker.
- Ontregelde slaap: Uit een meta-analyse uit 2005 blijkt een verhoogd risico op borstkanker voor vrouwen die 's nachts werken of in ploegendienst draaien.
- Onderzoek door het Amerikaanse bedrijf 23andMe lijkt op een genetische relatie tussen borstomvang en de kans op borstkanker te wijzen. Dezelfde genen die ervoor zorgen dat een vrouw grote borsten krijgt (onder meer SNP rs12173570), lijken ook de kans op borstkanker te vergroten.
Symptomen
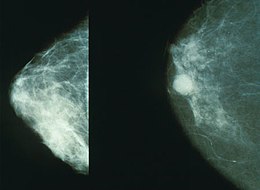
Meestal is de eerste klacht een voelbare knobbel in de borst, die meestal niet pijnlijk is. Soms kan er uitvloed uit de tepel bestaan (al dan niet bloederig), of is een tepel ingetrokken die dat normaal niet was. Het eerste teken van borstkanker kan soms ook een verandering van de huid van de borst of bij de tepel zijn (plotseling ontstane sinaasappelhuid van de borst of een zweertje). Knobbels onder de oksel kunnen op uitzaaiingen in de lymfeklieren (lymfkliermetastasen) duiden. Wanneer een knobbel in de borst gevoeld wordt, is de kans op kwaadaardigheid groter wanneer de huid boven de knobbel ingetrokken is, wanneer de knobbel vastzit aan de huid of aan de onderlaag (niet beweeglijk is), en wanneer de knobbel slecht afgrensbaar aanvoelt en een grillige vorm heeft.
Wanneer iemand een dergelijke klacht heeft, is het altijd het beste om naar de huisarts te gaan. Vaak blijkt er een goedaardig probleem te zijn, maar de huisarts is degene die dit het beste kan beoordelen. De beoordeling van dergelijke knobbels is soms moeilijk en zekerheid is vaak pas met andere onderzoeken (mammografie, echo-onderzoek, biopsie) te krijgen.
Met een mammografie die gedaan wordt in het kader van bevolkingsonderzoek, of vanwege een verhoogd risico op borstkanker, worden tegenwoordig ook borsttumoren gevonden die verder nog geen klachten gaven.
Vroege ontdekking
Hoe eerder ontdekt wordt dat iemand borstkanker heeft, hoe beter de behandelingsmogelijkheden zijn en hoe hoger de kans op overleving. Vroege ontdekking is dus belangrijk.
Zelfonderzoek


Lange tijd werd vrouwen geadviseerd regelmatig zelf hun borsten grondig en systematisch te onderzoeken. Door maandelijks zelfonderzoek van de borsten zou borstkanker vroeger opgespoord kunnen worden. Zo was het advies bij vrouwen die nog menstrueren dat het verstandig was dit onderzoek ongeveer een week na de menstruatie te doen, omdat borsten vóór de menstruatie enigszins gezwollen en pijnlijk kunnen zijn. Wanneer men de borsten maandelijks zou onderzoeken, zou men ook weten hoe de borsten "normaal" aanvoelen, en sneller doorhebben, of er iets veranderd is.
Er zijn nieuwe inzichten omtrent dit zelfonderzoek. Gebleken is dat zelfonderzoek van borsten wel goed is, maar dat het de kans om aan borstkanker te overlijden niet verkleint. Het levert geen gezondheidswinst op omdat vrouwen afwijkingen niet eerder ontdekken als ze maandelijks hun borsten onderzoeken. Bij het douchen, insmeren of voor de spiegel staan ontdekken vrouwen afwijkingen meestal vanzelf. Maandelijks systematische en grondig zelfonderzoek is daar niet voor nodig.
Er is geen onderzoek dat aantoont dat maandelijks zelfonderzoek van de borsten de kans kan verkleinen om aan borstkanker te overlijden. Vrouwen die wel regelmatig zelfonderzoek doen, hebben juist een grotere kans om onnodige ingrepen te ondergaan, omdat zij soms te veel voelen waardoor zij onnodig ongerust worden en medische hulp zoeken.
Bevolkingsonderzoek
In Nederland is er een bevolkingsonderzoek waarbij alle vrouwen tussen de 50 en 75 jaar elke twee jaar onderzocht worden op borstkanker. In België bestaat dit onderzoek eveneens tweejaarlijks voor alle vrouwen tussen 50 en 69 jaar. Dit gebeurt door het maken van een röntgenfoto van de borsten, een mammogram. De bedoeling hiervan is borstkanker in een zo vroeg mogelijk stadium op te sporen.
Bij vrouwen met een genetische of familiaire predispositie voor borstkanker geeft de straling die wordt opgelopen bij de mammografie een significant hoger risico op borstkanker. Om deze reden moet bij deze groep extra voorzichtig omgegaan worden met mammografie, met name wanneer zij nog jong zijn.
Het komt echter ook vaak voor, dat vrouwen na zo'n routinematige foto nog eens terug moeten komen voor nader onderzoek, omdat er een afwijking lijkt te zijn. Uiteindelijk kan dan blijken dat de vrouw toch geen borstkanker heeft en dat alle angst en ongerustheid "voor niets" is geweest.
Diagnose
Hoewel er met een lichamelijk onderzoek, een mammografie, een echo en/of een biopsie vaak al een zeer groot vermoeden op borstkanker kan bestaan, kan de definitieve diagnose pas gesteld worden door de patholoog, wanneer deze borstweefsel dat meestal door een operatie is weggehaald, onder de microscoop kan beoordelen.
Door onderzoek van de patiënt en van de tumor wordt de borsttumor ingedeeld in een bepaalde soort en categorie, en wordt het stadium van de borstkanker bepaald. Dit is belangrijk, om een mededeling te kunnen doen over de prognose en om te bepalen welke behandeling noodzakelijk is.
De patholoog kan bovendien enige speciale kleuringen doen van het weggehaalde weefsel, waardoor bepaald kan worden, of er speciale behandelingsmogelijkheden zijn, zoals hormoontherapie of immunotherapie. Ook zijn er sinds kort op microarray gebaseerde testen op de markt die de arts kunnen helpen bij de behandelingskeuze.
Soort borstkanker
Er bestaan verschillende soorten borstkanker, die ontstaan uit verschillende cellen.
- Ductaal carcinoma in situ (DCIS, 2,5%). Non-invasieve of in-situtumoren blijven in eerste instantie beperkt tot het klierweefsel van de borst.
- Lobulair carcinoma in situ (LCIS, 2,5%). Bij kanker die ontstaat in een melkklier spreekt men van een lobulair carcinoom.
- Invasief ductaal carcinoom (85%)
- Invasief lobulair carcinoom (10%)
En zeldzamer:
- Ziekte van Paget (3%)
- Mucineus infiltrerend of colloid carcinoom (2%)
- Tubulair carcinoom (1,2%)
- Inflammatoir carcinoom (mastitis carcinomatosa 1%)
- Phyllodes tumor (<1%)
TNM classificatie
De TNM-classificatie voor borstkanker is als volgt:
T (grootte van de tumor, dat wil zeggen van de knobbel in de borst)
| Code | Betekenis |
|---|---|
| Tis (T in situ) | er zijn kwaadaardige cellen, maar deze lijken nog niet invasief te zijn geworden. |
| T1 | de tumor is < 2 cm groot |
| T2 | de tumor is 2–5 cm groot |
| T3 | de tumor is > 5 cm groot |
| T4 | de tumor is ingegroeid in de borstwand of huid, of leidt tot ontstekingsverschijnselen. (NB de grootte van de tumor maakt dan niet uit). |
Het N-gedeelte van de TNM-classificatie, namelijk kenmerken van de lymfeklieren in de oksel, of soms van lymfeklieren op andere plaatsen dicht bij de borst, bestaat uit N0 (geen aanwijzingen voor uitzaaiingen in de lymfeklieren) en N1, N2 en N3 (in oplopende mate uitzaaiingen in de lymfeklieren).
Het M-gedeelte van de TNM-classificatie gaat over eventuele metastasen (uitzaaiingen) op afstand). Hierbij staat M0 voor geen aanwijzingen voor uitzaaiingen elders in het lichaam en M1 voor geconstateerde uitzaaiingen elders in het lichaam.
Stadium
Naast de indeling volgens de TNM-classificatie is nog een indeling in stadia mogelijk. Deze geven een beter beeld van de behandelingsmogelijkheden en van de prognose.
| stadium | beschrijving |
|---|---|
| stadium 0 | carcinoma in situ: dit komt overeen met Tis-stadium |
| stadium I | T1N0M0 (tumor < 2 cm, geen lymfeklieren aangedaan of uitzaaiingen) |
| stadium IIa | T2N0M0 (tumor 2–5 cm, geen lymfeklieren aangedaan of uitzaaiingen) of T1N1M0 (tumor < 2 cm, lymfeklieren wél aangedaan, geen uitzaaiingen) |
| stadium IIb | T3N0M0 (tumor > 5 cm, geen lymfeklieren aangedaan of uitzaaiingen) of T2N1M0 (tumor 2–5 cm, lymfeklieren wél aangedaan, geen uitzaaiingen) |
| stadium III | Alles meer dan stadium IIb, maar géén metastasen aangetoond (M0) |
| stadium IV | Alle T en N stadia, metastasen (uitzaaiingen) zijn aangetoond (M1) |
Hormoongevoeligheid / bijzondere kenmerken
De patholoog kan bepalen, of een tumor snel groeit (dan zijn er veel celdelingen te zien) of niet. Ook kan de patholoog zien, hoeveel de tumorcellen nog lijken op de oorspronkelijke borstcellen, met andere woorden hoe goed of slecht de cellen gedifferentieerd zijn. Slechte differentiatie en een snelle groei zijn ongunstig. De patholoog kan ook van elke tumor bepalen, of deze hormoongevoelig is (dan zijn er op de kankercellen receptoren te vinden voor de vrouwelijke hormonen oestrogeen en progesteron). Wanneer een tumor nog hormoongevoelig is, is dit in principe goed nieuws, omdat het onderdrukken van de vrouwelijke hormonen dan de groei van de tumor kan remmen. Hiervoor bestaan medicijnen.
Verder kan er getest worden op de Human Epidermal Growth Factor receptor-type 2 (HER2, ook wel aangeduid met HER2/neu of ErbB-2). Deze receptor is een eiwit dat voorkomt op de celmembraan, als hier te veel van is heeft deze cel een groeivoordeel. Bij de aanwezigheid van deze receptor is de prognose minder goed, omdat deze soort tumoren agressiever is. Er bestaat wel een medicijn, trastuzumab (Herceptin®) dat op deze receptor aangrijpt, waardoor ook dit soort kankercellen geremd kan worden.
Behandeling
Het is gebruikelijk dat vrouwen met borstkanker een combinatie van de hieronder genoemde behandelmethoden krijgen. De keuze en de volgorde van de verschillende behandelingen is onder meer afhankelijk van de kenmerken van de tumor, het stadium van de ziekte en van de leeftijd waarop borstkanker wordt geconstateerd. Op het moment dat er uitzaaiingen zijn aangetroffen in botten, longen, lever, hersenen en in zeldzame gevallen eierstokken, is de patiënt ongeneeslijk geworden. Dat betekent dat behandelingen het leven nog wel kunnen verlengen, maar de patiënt zal niet meer genezen en uiteindelijk met of aan borstkanker komen te overlijden.
Operatie
Bij de meeste patiënten met borstkanker is het noodzakelijk om de tumor chirurgisch te verwijderen. Bij redelijk kleine tumoren (stadium Tis, T1 en T2) kan men meestal kiezen tussen een borstsparende operatie (lumpectomie), waarbij alleen de tumor en een klein gebied eromheen weggehaald wordt, of een totale verwijdering van de borst (mastectomie). In het geval van een lumpectomie wordt vaak gebruik gemaakt van een tumorlokalisatie techniek. Dit helpt de chirurg om tijdens de operatie de tumor te vinden en met voldoende marge te verwijderen, met name als de tumor niet met de hand te voelen is. Standaard is het gebruik van een door de radioloog geplaatste metalen draad. Nieuwere technieken maken gebruik van een marker, die gelokaliseerd kan worden op basis van radio-activiteit of magnetisme. Na het verwijderen van het weefsel wordt de operatieholte gemarkeerd met clips. Dit helpt de radiotherapeut later bij het bepalen van het te bestralen gebied.
Bij grotere tumoren is er helaas soms geen keuze meer en moet de hele borst verwijderd worden. In het geval de tumor niet operabel is (te groot of ingegroeid in de borstwand), zal er vaak neo-adjuvante chemotherapie gegeven worden. Neo-adjuvant betekent dat het voorafgaand aan de operatie gegeven wordt, met als doel om de tumor kleiner te maken. Ook de losse, circulerende kankercellen worden hiermee aangepakt zodat de kans wordt verkleind dat de ziekte terugkomt.
Lymfeklieronderzoek tijdens de operatie
De lymfeklieren in de oksel bij de aangedane borst moeten meestal onderzocht worden door de patholoog, omdat hierin mogelijk kleine uitzaaiingen te vinden zijn, die men met het blote oog of met röntgenfoto's of echo's niet kan vaststellen. Vaak wordt hiervoor tijdens de operatie een schildwachtprocedure uitgevoerd, waarbij men de lymfeklier opspoort waar het tumorgebied direct op draineert (de schildwachtklier). Deze lymfeklier wordt verwijderd en nog tijdens de operatie onderzocht door de patholoog. Is deze lymfeklier niet aangedaan, dan wordt aangenomen dat de andere (er achterliggende) lymfeklieren ook vrij van metastasen zijn, en dan hoeft men deze niet te verwijderen. Wanneer de schildwachtklier wel aangedaan is, of wanneer men al vóór de operatie een zeer groot vermoeden heeft op aantasting van de lymfeklieren, worden alle (10 à 20) lymfeklieren uit de oksel verwijderd (het zogeheten okseltoilet).
Bestraling
Na een operatie volgt er meestal bestraling van de geopereerde borst. Radiotherapie verkleint de kans op het terugkomen van de tumor in de borst.
Medicatie
Hoewel borstkanker steeds meer voorkomt, neemt de sterfte af. Dit is voor een groot deel te danken aan de behandeling ervan met verschillende geneesmiddelen. Medicatie tegen borstkanker is bedoeld om de kans op terugkeer van de kanker te verkleinen, of om de hoeveelheid kankercellen te verminderen. Het advies om deze medicatie te gebruiken, hangt onder andere af van de leeftijd van de patiënt, het stadium van de borstkanker en speciale kenmerken van de borsttumor (bijvoorbeeld de hormoongevoeligheid).
De medicatie valt te verdelen in verschillende categorieën:
- Chemotherapie: behandeling met medicijnen die de celdeling remmen. De meest gebruikte middelen bij borstkanker zijn: 5-fluorouracil, epirubicine, cyclofosfamide, docetaxel en doxorubicine.
- Hormoontherapie: bij hormoongevoelige tumoren (aanwezigheid van oestrogeenreceptoren en/of progesteronreceptoren), behandeling met medicijnen die de werking van LHRH (ook wel GnRH genaamd) nabootsen, waardoor uiteindelijk de oestrogeen- en progesteronspiegels dalen, en de eierstokken niet meer functioneren. Bekendst: gosereline (Zoladex).
- Medicijnen hormoontherapie:
- Tamoxifen: een partiële oestrogeenantagonist (werkt remmend bij borstkanker, en stimulerend op endometrium, lipiden en bot.
- Aromataseremmers: niet-steroïdaal: anastrazol (Arimidex) en letrozol (Femara), steroïdaal: exemestaan (Aromasin).
- Targeted oftewel doelgerichte therapie:
- Geschikt voor tumoren met een overexpressie van Erbb2- ofwel Her2/neu- receptoren:
- trastuzumab (Herceptin): deze immunotherapie (antilichamen) is een monoklonale antistof, een eiwit, gericht op de Her2/neu -receptor.
- lapatinib (Tyverb): dit is een voorbeeld van de zogenaamde tyrosinekinaseremmers. Het is in tabletvorm.
- Gericht op de VEGF-receptor:
- bevacizumab (Avastin): dit is een monoklonale antistof die werkzaam is tegen vascular endothelial growth factor (VEGF). Het wordt ingezet als angiogeneseonderdrukker bij de behandeling van kanker om de aanleg van nieuwe bloedvaten (angiogenese) te onderdrukken
- Geschikt voor tumoren met een overexpressie van Erbb2- ofwel Her2/neu- receptoren:
Operabel
Tabel 1. Adjuvante systemische (chemo)therapie bij lymfklierpositieve-borstkanker zonder HER2-neu overexpressie.
| Premenopauzaal | Postmenopauzaal 50-59 | Postmenopauzaal 60-69 | Postmenopauzaal >70 | |
|---|---|---|---|---|
| ER+ en/of PgR+ | 5FEC + 5jr. tam. en/of LHRH | 5FEC + 2-3jr. tam. Gevolgd door 2-3jr. aromataseremmer | 2-3jr. tam. gevolgd door 2-3jr. aromataseremmer N≥4: 5FEC + 2-3jr. tam. gevolgd door 2-3jr. aromataseremmer | 2-3jr. tam. gevolgd door 2-3jr. aromataseremmer |
| ER- en PgR- | 5FEC | 5FEC | 5FEC | Geen advies mogelijk |
|
Een alternatief voor jonge patiënten zijn 6 kuren TAC, met G-CSF. | ||||
Tabel 2. Adjuvante systemische (chemo)therapie bij lymfklierpositieve-borstkanker met HER2-neu overexpressie.
| Premenopauzaal | Postmenopauzaal 50-59 | Postmenopauzaal 60-69 | Postmenopauzaal >70 | |
|---|---|---|---|---|
| ER+ en/of PgR+ | 4AC→P(12wkn) +1jr.Tras. en 5jr. tam. en/of LHRH | 4AC→P(12wkn) +1jr.Tras. en 5jr. aromataseremmer | 5jr. aromataseremmer. Indien N≥4: 4AC→P(12wkn) +1jr.Tras. en 5jr. aromataseremmer | 5jr. aromataseremmer. |
| ER- en PgR- | 4AC→P(12wkn) +1jr.Tras. | 4AC→P(12wkn) +1jr.Tras. | 4AC→P(12wkn) +1jr.Tras. | Geen advies mogelijk |
|
4AC→P(12wkn) +1jr.Tras. = 4 kuren doxorubicine en cyclofosfamide, gevolgd door 4 kuren van 3 weken of 12 wekelijkse kuren paclitaxel, en 1 jaar trastuzumab. Een alternatief voor 4AC→P(12wkn) +1jr.Tras. zijn 5 kuren FEC, gevolgd door 1 jaar trastuzumab. | ||||
Tabel 3. Adjuvante systemische therapie bij lymfkliernegatieve-borstkanker zonder HER2-neu overexpressie. Gebaseerd op tumorgrootte en differentiatiegraad (SBR).
| SBR I | SBR II | SBR III | |
|---|---|---|---|
| ≤ 1 cm | Geen | Geen. ≤ 35 jaar als N+-patiënten in tabel 1. | Geen. ≤ 35 jaar als N+-patiënten in tabel 1. |
| 1–2 cm | Geen. ≤ 35 jaar als N+-patiënten in tabel 1. | Geen. ≤ 35 jaar als N+-patiënten in tabel 1. | Als N+-patiënten in tabel 1. |
| 2–3 cm | Geen. ≤ 35 jaar als N+-patiënten in tabel 1. | Als N+-patiënten in tabel 1. | Als N+-patiënten in tabel 1. |
| ≥3 cm | Als N+-patiënten in tabel 1. | Als N+-patiënten in tabel 1. | Als N+-patiënten in tabel 1. |
Tabel 4. Adjuvante systemische therapie bij lymfkliernegatieve-borstkanker met HER2-neu overexpressie. Gebaseerd op tumorgrootte en differentiatiegraad (SBR).
| SBR I | SBR II | SBR III | |
|---|---|---|---|
| ≤ 1 cm | Geen | Geen. ≤ 35 jaar als N+-patiënten in tabel 2. | Geen. ≤ 35 jaar als N+-patiënten in tabel 2. |
| 1–2 cm | Geen. ≤ 35 jaar als N+-patiënten in tabel 2. | Geen. ≤ 35 jaar als N+-patiënten in tabel 2. | Als N+-patiënten in tabel 2. |
| 2–3 cm | Geen. ≤ 35 jaar als N+-patiënten in tabel 2. | Als N+-patiënten in tabel 2. | Als N+-patiënten in tabel 2. |
| ≥3 cm | Als N+-patiënten in tabel 2. | Als N+-patiënten in tabel 2. | Als N+-patiënten in tabel 2. |
Psychosociale zorg
Borstkanker heeft niet alleen een invloed van medische aard, maar het heeft ook een invloed op het leven, het lichaam en het zelfvertrouwen. Pink Ribbon is een organisatie die zijn aandacht onder andere vestigt op de begeleiding van (ex-)patiënten die nood hebben om hun verhaal kwijt te kunnen. Dit doen ze door projecten te ondersteunen die psychosociale zorgen bieden aan patiënten en hun omgeving.
| Bronnen, noten en/of referenties |
